Lo que sabemos sobre el primer fármaco ruso para el coronavirus
Salud / / December 29, 2020

N + 1 - ciencia popular edición sobre lo que está sucediendo en ciencia, ingeniería y tecnología en este momento.
El primer medicamento ruso para la enfermedad por coronavirus "Avifavir" recibió la aprobación del Ministerio de Salud. El desarrollador del fármaco promete que enviará los primeros lotes de su fármaco a los hospitales el 11 de junio. Descubrimos de dónde provienen estas píldoras amarillas, cómo funciona el medicamento, qué ya ha pasado las pruebas y es posible decir con certeza que tenemos una cura para COVID-19.
De dónde vino
Avifavir es el nombre comercial de un fármaco ruso desarrollado por el Fondo de Inversión Directa de Rusia (RDIF) y el grupo de empresas ChemRar. Sin embargo, el ingrediente activo de la droga no fue inventado. En Rusia.
Su nombre común internacional es favipiravir. Desarrollado por empleados de la empresa japonesa Toyama ChemicalToyama Chemical Co Ltd - una subsidiaria de FUJIFILM Pharmaceuticals Corporation.
Por su estructura química, el favipiravir es un derivado
Favipiravir Ácido 6 - fluoro - 3 - oxo - 3,4 - dihidropirazina - 2 - carboxílico o pirazinacarboxamida. Durante una revisión de una biblioteca química, los empleados de Toyama descubrieron que esta sustancia puede tener actividad contra el virus de la influenza: células infectadas con un virus, favipiravir se convierte en una forma activada que inhibe la actividad de una importante enzima viral ARN-polimerasa dependiente de ARNEnfermedad por coronavirus 2019 (COVID-19): Manejo en adultos hospitalizados.Si se desactiva la ARN polimerasa, los virus de la influenza pierden la capacidad de imprimir su material genético, ARN, en las células infectadas. Como resultado, se detiene la producción del virus que ya ha entrado en las células. Esta es la singularidad del fármaco: por lo general, los fármacos antivirales solo pueden evitar que los virus entren en las células.
La ARN polimerasa dependiente de ARN no solo se encuentra en virus gripe, pero también en todos los virus de ARN. Además, el dominio catalítico de la ARN polimerasa - este es el nombre de la parte de la molécula, gracias a la cual la enzima puede funcionar en principio - está estructurado de la misma manera en todos los virus ARN. Y dado que el favipiravir se une precisamente al dominio catalítico de la ARN polimerasa, los japoneses tenían motivos para considerar esta sustancia como un agente antiviral de una amplia gama.Favipiravir (T - 705), un inhibidor de amplio espectro de la ARN polimerasa viral espectro de acción.
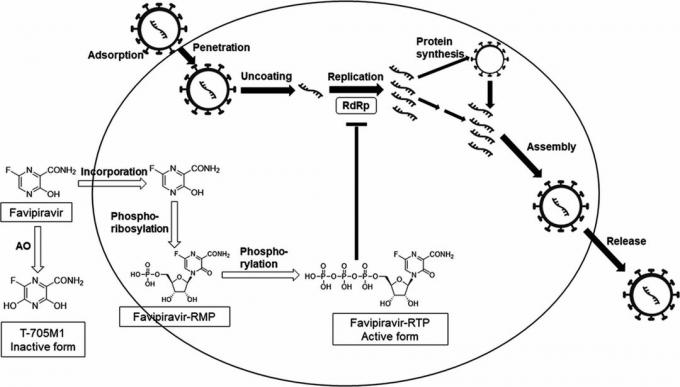
Los empleados de Toyama registraron favipiravir con la marca Avigan y comenzaron a investigar la actividad de un fármaco prometedor en los virus de ARN.Favipiravir (T - 705), un nuevo inhibidor de la polimerasa de ARN viral: desde los virus de la influenza tipo A y B hasta el virus del Ébola. Los resultados fueron mixtos. Por ejemplo, en el caso del virus del Ébola, resultó que la droga funcionó en monos.Eficacia antiviral de favipiravir contra el virus del Ébola: un estudio traslacional en macacos cynomolgus, pero cuando se aplica en humanos, el resultadoLos tiempos de supervivencia mejoraron en los pacientes con ébola tratados con favipiravir no fue muy impresionante. Por un lado, la tasa de mortalidad en 73 pacientes guineanos tratados con favipiravir fue menor que en los pacientes que habían probado para sanar De otras maneras. Por otro lado, la diferencia no fue tan grande: 42.5 por ciento versus 57.8 por ciento, es decir, imposible asegurarse de que esto no sea solo un artefacto de conteo aleatorio asociado con el hecho de que la muestra de pacientes fue muy pequeña. Sin embargo, el Gobierno de Guinea aprobóJapón envía favipiravir, fármaco de Fujifilm para la gripe, a más de 40 países para ensayos de Covid-19 este medicamento se usa como tratamiento estándar para el virus del Ébola.
En la patria de la droga, en Japón, Avigan logró Registrarse solo en 2014, y solo contra nuevas cepas del virus de la influenza. Avigan no se ha utilizado contra la gripe estacional.

Además, el medicamento fue aprobado no solo contra la "nueva" influenza, sino exclusivamente para situaciones en las que los medicamentos antivirales existentes eran ineficaces, es decir, como último recurso. Durante seis años desde el momento de la aprobación, tal situación no ha surgido ni una sola vez, por lo que en las condiciones de una verdadera epidemia de gripe, el medicamento nunca se usó.
Una revisión de 29 ensayos clínicos (4299 participantes), seis de los cuales eran ensayos de fase 2 y 3 (ya en evaluación) eficacia del fármaco) mostró que favipiravir "presenta un perfil de seguridad favorable": la proporción de efectos secundarios graves arregladoUna revisión de la seguridad del favipiravir: ¿un tratamiento potencial en la pandemia de COVID-19? 0,4 por ciento. Sigue habiendo problemas de seguridad droga todavía queda.
Los investigadores japoneses que estudian las perspectivas de usar el medicamento para la influenza grave enfatizaronFavipiravir, un medicamento contra la influenza contra las infecciones por virus ARN potencialmente mortalesque Avigan está contraindicado en mujeres embarazadas: el fármaco tuvo efectos teratogénicos y embriotóxicos en animales. Otros posibles problemasFavipiravir (Estados Unidos: no disponible comercialmente; consulte Restricciones de prescripción y acceso): Información sobre medicamentos: disminución del apetito, náuseas, vómitos, aumento de la concentración de ácido úrico en sangre (hiperuricemia) y daño hepático.
Leyendo ahora🔥
- Las consecuencias del coronavirus pueden durar toda la vida. Esto es lo que se sabe al respecto.
Favipiravir y COVID-19
En marzo de 2020, Zhang Xinmin, director del Centro Nacional para el Desarrollo de Biotecnología, que forma parte del Ministerio de Salud de China, dijoFavipiravir muestra una buena eficacia clínica en el tratamiento de COVID-19: oficialque el favipiravir "ha demostrado una buena eficacia clínica contra la nueva enfermedad por coronavirus (COVID-19)". Según los datosTratamiento experimental con favipiravir para COVID - 19: un estudio de control abierto al menos un estudio abierto, no aleatorizado, 35 pacientes chinos con enfermedad por coronavirus tratados con favipiravir (el estudio no dijo sobre qué medicamento se discutió (el Avigan original o un medicamento chino con el mismo ingrediente activo), se recuperó más rápido y sufrió menos complicaciones que 45 pacientesque fueron tratados con otros medicamentos (lopinavir y ritonavir).
Actualmente, se está evaluando la efectividad del fármaco contra COVID-19Enfermedad por coronavirus 2019 (COVID-19): Manejo en adultos hospitalizados en ensayos clínicos en Japón. 9 de abril FUJIFILM anunciadaFujifilm anuncia el inicio de un ensayo clínico de fase II de su medicamento antiviral contra la influenza “Avigan® Tablet” para pacientes con COVID-19 en los EE. UU. Al comienzo de la segunda fase de los ensayos clínicos de Avigan, que tendrá lugar en los Estados Unidos, participarán en el ensayo 50 pacientes con enfermedad por coronavirus. Según algunos datos extranjeros, en abril-mayo, se probó favipiravir en 16 ensayos clínicos más, pero ninguno ensayo clínico completado que muestra que favipiravir o Avigan son eficaces contra el coronavirus enfermedad, no.
Droga rusa
Cualquier medicamento consta de un principio activo y un relleno (forma farmacéutica terminada). El medicamento antiviral ruso contiene el mismo ingrediente activo.El primer fármaco ruso contra el coronavirus recibió la aprobación del Ministerio de Saludcomo la droga japonesa, es decir, 200 miligramos de favipiravir por tableta. Como en una conversación con "N + 1" señaló el representante del RDIF Arseny Palagin, el relleno de la droga rusa es el suyo. Las instrucciones dicen que los excipientes incluyen celulosa microcristalina, croscarmelosa de sodio, dióxido de silicio coloidal, estearato de magnesio y povidona K-30. El período de protección de la patente para el Avigan japonés original expiró en 2019, por lo que el medicamento puede considerarse producido legalmente. genérico.
Los ensayos clínicos rusos de avifavir tampoco han finalizado todavía. Completada sólo la primera y segunda etapa de un estudio multicéntrico aleatorizado, confirma el interlocutor "N + 1" del RDIF. La primera etapa involucró a 60 personas, 20 de ellas se incluyeron en el grupo de control, que fue tratado con métodos estándar. No se revelaron datos sobre la composición por edades y la gravedad de la afección de los sujetos.
Esto es lo que se informaRDIF y ChemRar Group of Companies entregarán 60.000 cursos de avifavir, el primer fármaco registrado en la Federación de Rusia contra COVID-19, a hospitales rusos en junio los propios desarrolladores sobre los resultados de estas pruebas:
- nuevos efectos secundarios además de los que los japoneses registraron hace muchos años, no revelaron;
- después de cuatro días de tratamiento en el 65 por ciento de las personas en el grupo experimental prueba de coronavirus dio un resultado negativo (en el grupo de control, tales casos fueron alrededor del 30 por ciento);
- después de tres días, el 68 por ciento de las personas del grupo experimental volvió a la temperatura normal (en el control, esto sucedió al sexto día).
El Ministerio de Salud aprobó el inicio de la tercera fase de pruebas de "Avifavir" el 1 de mayo de 2020. En esta etapa, según los datosRegistro estatal de medicamentos en la página web del Registro Estatal de Medicamentos deberán participar un total de 390 personas. Los mismos datos muestran que el favipiravir está siendo probado por otras dos empresas rusas: Drugs Technology (parte del grupo R-Pharm) y Promomed. Ambas empresas comenzaron a realizar pruebas a finales de mayo.
Aunque los ensayos no están completados y solo se conocen datos parciales sobre la efectividad, el Ministerio de Salud permitió que el medicamento se registrara anticipadamente, de acuerdo con el procedimiento acelerado adoptado en virtud del decreto.Resolución del Gobierno de la Federación de Rusia de 3 de abril de 2020 No. 441 Gobierno de la Federación de Rusia con fecha 3 de abril de 2020 No. 441. Este decreto establece que “una reducción en el volumen de <...> exámenes” es permisible “en condiciones de amenaza de emergencia y liquidación emergencia».
Entonces el fabricante ya prometeRDIF y ChemRar Group of Companies entregarán 60.000 cursos de avifavir, el primer fármaco registrado en la Federación de Rusia contra COVID-19, a hospitales rusos en junio para fines de la próxima semana, lleve los primeros lotes de píldoras a los hospitales.
En las instruccionesInstrucciones para el uso médico del medicamento "Avifavir". para el medicamento está escrito que fue "preparado sobre la base de una cantidad limitada de datos clínicos sobre el uso del medicamento y se complementará a medida que se disponga de nuevos datos". Sin embargo, ya se han identificado contraindicaciones. Al igual que con el Avigan japonés, esto es planificación del embarazo, el embarazo y el período de lactancia: el genérico también es potencialmente teratogénico. Los pacientes con gota e hiperuricemia deben usar el medicamento con precaución. Además, la lista de contraindicaciones para el medicamento genérico ruso se complementó con hipersensibilidad al principio activo, edad hasta 18 años, insuficiencia hepática y renal grave.
El medicamento no se entregará a las farmacias: de acuerdo con las instrucciones, el medicamento solo se puede usar en hospitales.
Cual es el resultado
Avifavir es un fármaco genérico de Favipiravir, que tiene un mecanismo de acción distinto y está siendo sometido a ensayos clínicos en Rusia y en el extranjero.
Los resultados de los ensayos clínicos provisionales muestran que el fármaco es prometedor: en los pequeños muestras que lograron comprobar, el efecto terapéutico, a juzgar por las declaraciones de los desarrolladores, para determinar logrado. Pero hasta que se completen los ensayos clínicos y los resultados se publiquen en revisión por pares revistas internacionales, no podemos estar completamente seguros de que Avifavir realmente ayude contra el coronavirus enfermedad. El servicio de prensa de ChemRar, el desarrollador del fármaco, no respondió las preguntas de N + 1 en el momento de la publicación de este texto.
Ahora no tenemos medicamentos que actúen de manera deliberada y efectiva contra el virus SARS-CoV-2. Todos los aspirantes a este título ahora son sustancias conocidas antes de la aparición del nuevo coronavirus, que en clínica Las pruebas (que acaban de comenzar) muestran constantemente algún efecto positivo con una serie de restricciones. Hay dos de ellos ahora mismo.
El primero es Remdesivir, que llegó a las portadas en mayo, un medicamento que incluso antes de la epidemia de COVID-19 estaba destinado a tratar otra infección de coronavirus, Síndrome respiratorio de Oriente Medio (MERS). El regulador estadounidense aprobó el uso clínico de Remdesivir sin esperar su finalización formal ensayos de fármacos, - la presencia de un efecto estable en los datos preliminares de la investigación convenció a los médicos funcionarios. Esta situación fue comparadaTodos los ojos puestos en Galaad con registro temprano AZTZidovudina, la primera cura para el VIH.
Al mismo tiempo, "Remdesivir" nunca reclamó el estado de "bala de plata": las pruebas muestranRemdesivir para el tratamiento de Covid-19 - Informe preliminarque no puede ayudar a las personas con síntomas graves, que necesitan ventilación mecánica de los pulmones, y para aquellos con síntomas más leves, reduce el tiempo de enfermedad en cuatro días. Muchos otros efectos, por ejemplo, la reducción de la mortalidad de la enfermedad en comparación con otros fármacos, no se mostraron con significación estadística en estos ensayos. La muestra de ensayos de Remdesivir, informada a fines de mayo por el New England Journal of Medicine, fue de 1.059 personas.
Elena Verbitskaya
Jefe del Departamento de Estadísticas Biomédicas de la Universidad Médica Estatal de San Petersburgo que lleva el nombre del académico I. pags. Pavlova.
60 sujetos: ¿es mucho o poco?
El número de sujetos necesarios para probar la eficacia de un fármaco se calcula utilizando fórmulas especiales que tienen en cuenta muchas variables: por ejemplo, características de los indicadores que se supone que deben tenerse en cuenta, su propagación, el nivel de desviación de los indicadores del grupo de control, que se considerarán clínicamente significativo.
Se asignan indicadores que se tendrán en cuenta durante las pruebas. El principal suele ser la mortalidad. En el caso de las infecciones respiratorias se utilizan indicadores integrales, que tienen en cuenta, por ejemplo, el número de días con fiebre, el tiempo en cuidados intensivos o unidad de cuidados intensivos, en ventilación mecánica y tos. Todos ellos se convierten en puntos según una fórmula determinada, y luego se comparan los puntos del grupo experimental con los puntos del grupo de control.
Para algunas investigaciones, 20 sujetos serán suficientes. Para algunos, 2000 no es suficiente.
Se pueden realizar ensayos piloto en un grupo pequeño antes de los ensayos clínicos. No es infrecuente que se produzca una situación en la que un efecto que se encuentra en un grupo de varias docenas de personas posteriormente se "erosiona" en grupos grandes.
El favipiravir, como Remdesivir, no se desarrolló originalmente como un remedio específicamente contra el nuevo coronavirus. El medicamento hace muchos años, tanto que su patente había expirado, se adaptó para el tratamiento de la influenza (virus estrictamente nuevos, no enfermedades estacionales) y se probó contra los virus del Ébola y Zika.
Sí, los investigadores rusos parecen haber captado el efecto de su uso en el tratamiento. COVID-19 - pero hasta ahora, en una pequeña muestra de 60 personas, no hay información detallada sobre los métodos de selección y composición de los cuales.
Entonces parece que tenemos pastillas. Y para asegurarse de que se trata realmente de un medicamento, tendrá que esperar un poco más.

Coronavirus. Número de infectados:
6 661 888
en el mundo441 108
En RusiaLeer también🦠
- ¿Cuánto tiempo durará la inmunidad al nuevo coronavirus?
- 6 trucos que realmente no protegen a los gérmenes
- Cómo se verían las nuevas olas de una pandemia

